|
了解美临达 美临达医疗,专注于企业资质咨询,可提供ISO体系认证、医疗器械化妆品、消毒产品、食品相关资质及配套服务。 |
 |
专业的服务团队 美临达医疗拥有一支专业的技术服务团队,平均行业经验5年以上,人员素质良好,可提供优质的服务。 |
 |
合理的费用预算 美临达医疗,通过提高团队效率,压缩服务成本,降低服务报价,为客户提供质优价廉的专业服务。 |
 |
良好的售后体验 美临达医疗承诺售后服务,均可良好兑现,为客户提供更多咨询、工具和参考意见,帮助客户解决更多问题。 |
医疗器械资质
-----------------------------------------------
专、快、优、省
 |
|
医疗器械分类界定 |
|
美临达专业办理进口/国产医疗器械分类界定。
提供如下服务: 1.电话沟通,全面了解客户需求; 2.制定服务方案,计划安排医疗器械分类及界定时间费用; 3.专人对接,一对一服务,撰写申请相关材料; 4.与客户沟通,安排申请与受理事宜; 5.跟进审核进度,完成不符合项整改; 6.取得医疗器械分类界定告知书。 |
||
|
|
||
|
|
||
|
|
||
|
|
|
医疗器械分类界定服务流程
|
||
|
|
|
医疗器械分类界定服务流程:
(1)企业咨询美临达:
客户咨询美临达客服,了解客户需求。
(2)定制服务方案:
美临达根据客户详细需求,定好服务方案,制定办理医疗器械分类界定时间费用计划。
(3)合同阶段:
客户与美临达签订技术服务合同,支付服务款项,美临达即开始服务。
(4)提交受理阶段:
美临达协助申请企业准备好医疗器械分类界定申请资料后,就可以向药监部门提出生产许可申请。药监部门对医疗器械分类界定告知书申请资料进行审查,并对申请资料发出补正意见。美临达协助客户沟通并完成资料整改补正。 (5)批准发布: 申请企业对所有提出的不符合项进行整改后,符合要求的,药监部门将颁发医疗器械分类界定告知书证书。
|
|
医疗器械分类界定资料清单
|
||
|
|
|
医疗器械分类界定文件清单
1.医疗器械界定申请表
2.产品照片和/或产品结构图
3.产品技术要求及产品说明书(样稿)
4.进口上市证明材料(如有)
5.资料真实性自我保证声明;
6.其他与产品分类界定有关的的材料。 |
|
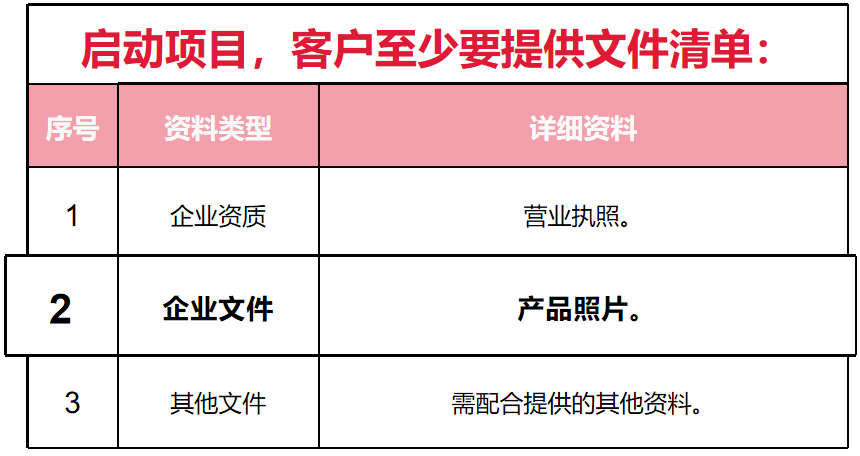
企业至少提供文件清单
|
||
 |
||