 联系我们
联系我们
 18210828691
18210828691
在深圳如何办理持棒钳一类医疗器械备案?
美临达医疗专业办理第一类医疗器械备案,联系电话18210828691(微信同)
产品信息:
|
产品名称 |
持棒钳 |
|
类别 |
一类医疗器械/诊断试剂 |
|
产品描述 |
通常由钳柄、钳头和鳃轴螺钉组成,钳头内表面多设有齿,钳柄之间可设置锁合装置。一般采用不锈钢材料制成。非无菌提供。使用前由使用机构根据说明书进行灭菌或消毒(如适用)。不在内窥镜下使用。 |
|
预期用途 |
用于骨科手术中夹持并固定骨骼、植入物,或夹持器械。 |
持棒钳,在2021版《医疗器械分类目录》/《诊断试剂分类目录》中属于一类医疗器械或诊断试剂,不同于二类医疗器械注册,国产一类器械不需要注册及生产许可证,仅须到深圳市市场监督管理局办理产品备案及生产,即可生产销售。这里所说的备案,指的是第一类医疗器械产品备案及第一类医疗器械生产备案,分别获得第一类医疗器械产品备案凭证及第一类医疗器械生产备案凭证。
那么在深圳如何办理产品备案凭证及生产备案凭证呢?下面小编逐步给大家讲解:
1. 主管部门:
深圳市市场监督管理局,可以在深圳市政务服务网(https://www.gdzwfw.gov.cn/portal/index?region=440300)上检索“第一类医疗器械产品备案”及“第一类医疗器械生产备案”即可找到相关事项及主管部门。
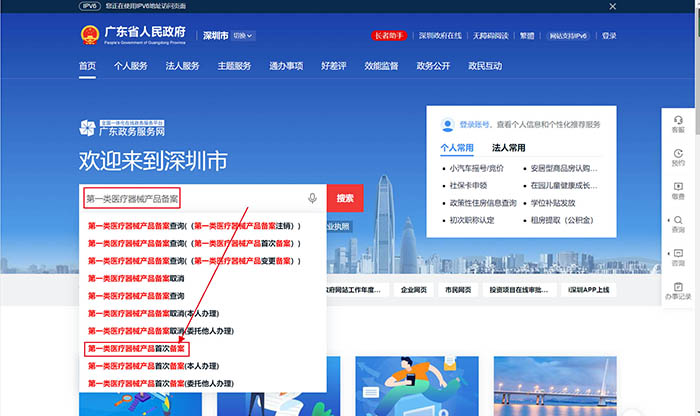
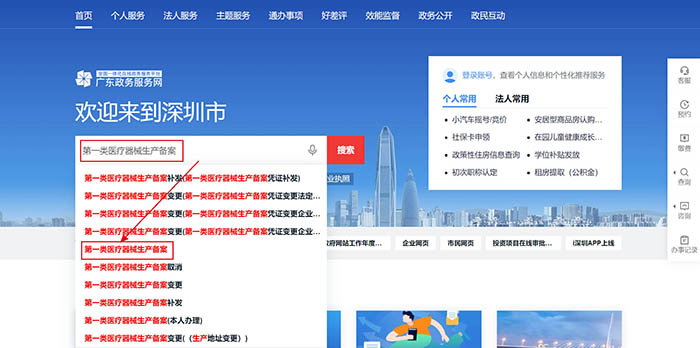
2. 办事指南:
第一类医疗器械备案申请资料为全国统一,但深圳地区有一些地方特色,所以检索到办事指南,是办理成功的关键一步,可以在当地政务服务网上检索“第一类医疗器械产品备案”及“第一类医疗器械生产备案”即可找到相关事项的办事指南。
全国各地备案办事指南链接http://www.medlinda.com
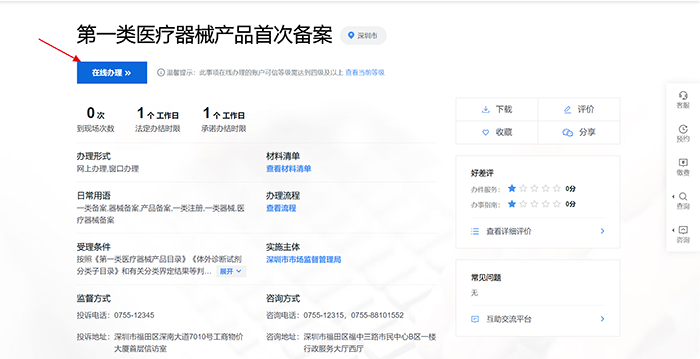
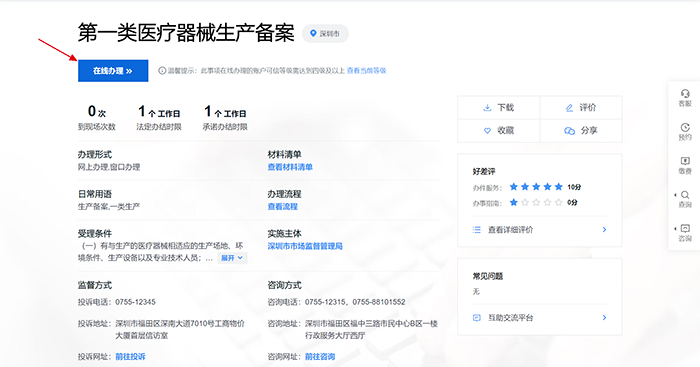
3. 办理方式:
深圳市第一类医疗器械备案一律实行网上办理:备案人先将准备好的资料上传官方系统,即政务服务网系统,注册好账号实名认证后即可上传;总之,备案人先将准备好的资料按要求上传主管部门,由主管部门进行审阅,直到资料符合要求后,才会发放备案电子证书。
4. 资料准备:
下一步即可认真准备相关资料(不同地区资料要求略有不同,以下信息仅供参考):
产品备案资料:
(1)备案表:一般在政务服务网下载,或在国家药品监督管理部门官方网站系统填写,填写后打印盖章递交原件。
(2)关联文件,即公司营业执照。
(3)持棒钳技术要求:
技术要求指标:
1)产品规格型号及划分说明/2)外观/3)尺寸/4)理化性能/5)使用性能
一般选取以上指标,参考同类产品性能,指定相关指标及检验方法。(提示:请依据公司产品制定)
(4)检验报告
需为委托检验报告或全性能自检报告,如果厂家有自检能力,可选择自检。本产品建议委托有资质的检测机构进行全项目的检测。
(5)产品说明书及标签
根据医疗器械说明书及标签编写指导原则编写。
(6)生产制造信息
详细描述生产过程相关情况。
(7)符合性声明
声明符合备案的要求,符合产品目录及相关法规及标准,声明提交资料的真实性。
准备好以上资料,即可向深圳市市场监督管理局申请第一类医疗器械产品备案。
生产备案资料:
(1) 生产备案表
在政务网下载,或在国家药品监督管理局网站填写,打印盖章后递交原件;
(2) 法人身份证复印件
(3) 技术负责人、生产负责人及质量负责人学历、职称证明及身份证明
(4) 生产质量负责人等一栏表
(5) 厂房产权证明和租赁协议
(6) 主要生产设备和检验设备目录
主要生产设备:一般包含:生产流水线等。(提示,请依据产品生产工艺确定)
主要检验设备:一把包含:游标卡尺、钢直尺、性能测试仪、温度计等(提示,请依据检验项目确定)
(7) 质量手册和程序文件,可根据医疗器械生产质量管理规范编写,也可根据ISO 13485-2016编写。
(8) 产品生产工艺
(9) 经办人授权书及身份证复印件
准备好以上文件,即可向深圳市市场监督管理局申请第一类医疗器械生产备案。
在深圳市备案持棒钳备案,选美临达医疗!
美临达医疗,专注于医疗器械注册!有丰富的行业经验,欢迎联系18210828691咨询。
美临达官方网站:www.medlinda.com
以上内容来自第三方机构或网站,由美临达医疗理发布。仅用于知识分享,不作为广告用途,如有不当或侵权,请联系美临达修改或删除。