 联系我们
联系我们
 18210828691
18210828691







【图文】医用冷敷贴一类医疗器械备案指南:快速合规,安全守护
在医疗健康领域,医用冷敷贴作为一种常见的物理治疗方法,广泛应用于各种疼痛、肿胀和炎症的缓解。为了确保医用冷敷贴的质量和安全性,满足国家相关法规和标准的要求,进行一类医疗器械备案成为了必不可少的步骤。本文将为您详细解读医用冷敷贴一类医疗器械备案的定义、重要性及办理流程,助您轻松实现合规上市。
#热门话题# 医用冷敷贴备案,守护健康,合规先行!
一、医用冷敷贴一类医疗器械备案定义
医用冷敷贴一类医疗器械备案是指将医用冷敷贴产品按照国家相关法规和标准进行分类、审查、批准和备案的过程。经过备案的医用冷敷贴将获得医疗器械备案凭证,具备在市场上合法销售和使用的资格。
二、医用冷敷贴一类医疗器械备案的重要性
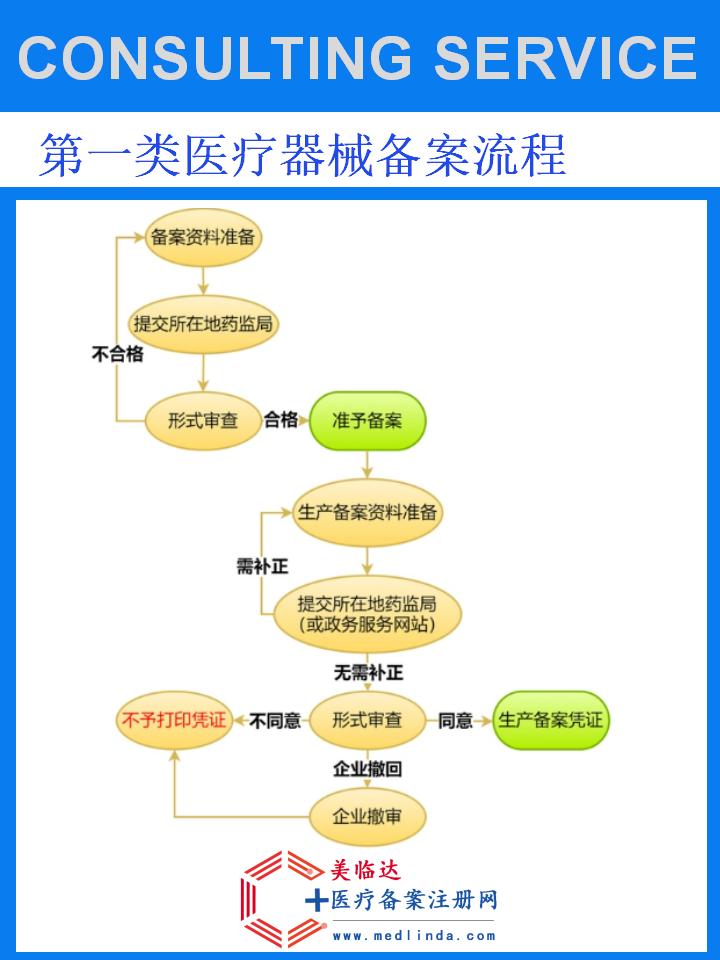
三、医用冷敷贴一类医疗器械备案办理流程
四、总结
医用冷敷贴一类医疗器械备案是确保产品合规上市的重要步骤。通过了解法规与标准、准备申请材料、提交申请并接受审核等流程,企业可以顺利获得备案凭证,实现合规上市。让我们携手合作,共同为医疗健康领域的健康发展贡献力量!