





【图文】下肢固定器械备字号审批流程与要求:合规上市,稳健前行
在#医疗健康#、#康复辅助#等热门话题的推动下,下肢固定器械作为促进下肢康复、提升患者生活质量的重要医疗设备,其市场需求持续增长。然而,要让下肢固定器械合法、安全地进入市场,获取备字号(即医疗器械备案凭证)并遵循严格的审批流程是不可或缺的一环。本文将为您详细阐述下肢固定器械备字号审批的流程与要求,助您稳健前行,合规上市。
定义篇:下肢固定器械的角色
下肢固定器械,专为下肢设计,旨在通过稳定的支撑与固定,帮助患者缓解下肢疼痛、促进骨折愈合、改善步态等。广泛应用于骨科、康复科等多个医疗领域,是下肢康复治疗中不可或缺的工具。
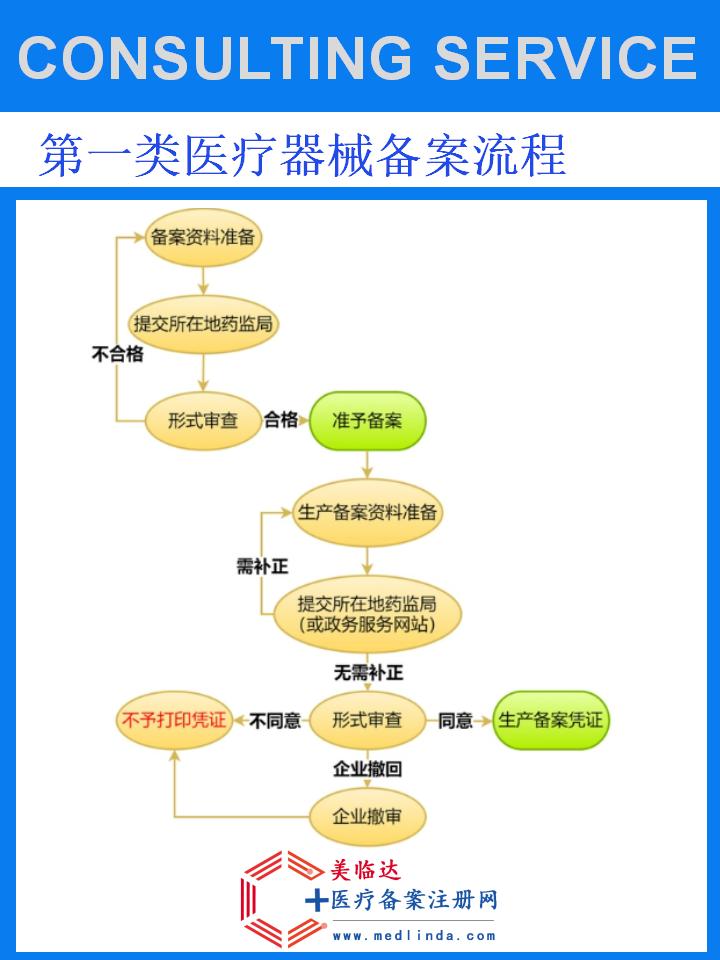
备字号审批流程
1. 前期准备
-
企业资质:确保企业具备合法的营业执照、医疗器械生产或经营许可证等资质,满足医疗器械生产或经营的基本条件。
-
产品资料准备:收集并整理下肢固定器械的设计图纸、生产工艺流程、原材料证明、质量检测报告、产品说明书、使用说明书等关键资料。
-
分类判定:根据《医疗器械分类目录》,准确判断下肢固定器械的分类,确认其属于一类或二类医疗器械,并了解相应的审批要求。
2. 提交申请
-
选择申请途径:根据产品分类和所在地政策,选择向国家药品监督管理局(NMPA)或地方药品监督管理部门提交备案申请。
-
填写申请表:按照要求填写并提交下肢固定器械的备案申请表,同时附上完整的产品资料。
-
缴纳费用:根据规定缴纳备案申请费用。
3. 审核与评估
-
形式审查:监管部门对提交的资料进行形式审查,确认资料齐全、格式规范。
-
实质审查:对产品的安全性、有效性、质量可控性进行评估,必要时会进行现场核查或要求补充资料。
4. 审批与发证
-
审批通过:经审核通过后,企业将获得下肢固定器械的备字号(即医疗器械备案凭证),产品可合法上市销售。
-
信息公开:备案信息将在国家药品监督管理局网站等平台上公开,接受社会监督。
审批要求
-
真实性:提交的所有资料必须真实、准确、完整,不得有虚假内容。
-
合规性:产品必须符合国家医疗器械相关法律法规、标准和技术要求。
-
安全性:产品应确保使用过程中的安全性和有效性,不会对患者造成不必要的伤害。
结语
下肢固定器械备字号审批是确保产品合规上市、保障患者安全的重要环节。通过遵循严格的审批流程和要求,企业能够提升产品竞争力,赢得市场认可。在未来的发展中,让我们携手并进,共同推动下肢固定器械行业的健康发展,为更多患者带来康复的希望。
 联系我们
联系我们
 18210828691
18210828691







