 联系我们
联系我们
 18210828691
18210828691
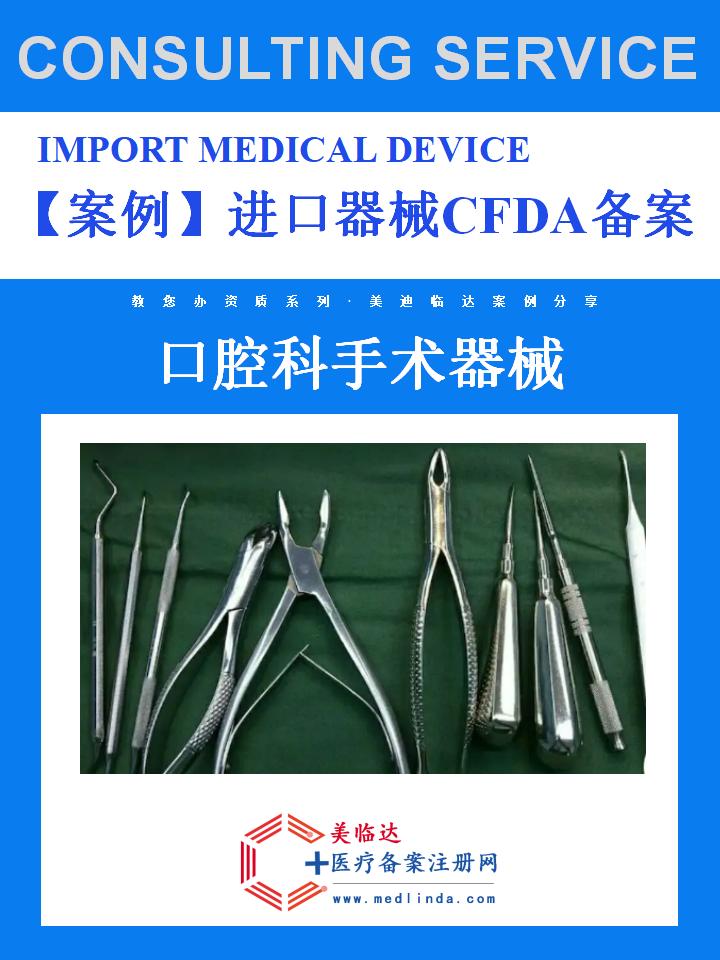



【案例】进口口腔科手术器械医疗器械备案凭证申请方式:专业导航,畅通无阻
在口腔医学领域,手术器械的精度与安全性直接关系到患者的治疗效果与康复过程。随着国际医疗技术的交流与融合,进口口腔科手术器械以其先进的技术、卓越的性能和人性化的设计,成为众多口腔医院和诊所的首选。然而,将这些高质量的医疗设备引入中国市场,必须跨越一道重要的门槛——获得进口医疗器械备案凭证。本文将以实际案例为基础,深入探讨进口口腔科手术器械医疗器械备案凭证的申请方式,并融入#医疗健康国际化#、#医疗器械合规经营#等热门话题,为相关企业提供详尽的指导与参考。
进口口腔科手术器械的备案,不仅是遵守中国法律法规的必然要求,更是保障医疗器械质量安全、维护患者健康权益的重要措施。通过正规渠道完成备案,企业可以确保产品符合中国市场的监管标准,顺利进入市场并获得消费者的认可。同时,备案过程也是企业展示产品实力、提升品牌形象的重要机会。
进口口腔科手术器械医疗器械备案凭证,是指由国家药品监督管理局(NMPA)或其指定机构颁发的,允许特定型号的进口口腔科手术器械在中国境内销售的许可证明。该凭证是产品合法销售、医院采购及患者使用的重要依据,也是企业在中国市场开展业务的基础。
在申请之前,企业需全面了解中国关于进口医疗器械的法律法规、政策文件及最新动态。这包括但不限于《医疗器械监督管理条例》、《进口医疗器械注册与备案管理办法》等,确保申请过程符合法律要求。
申请资料是备案申请的核心,企业需精心准备以下关键资料:
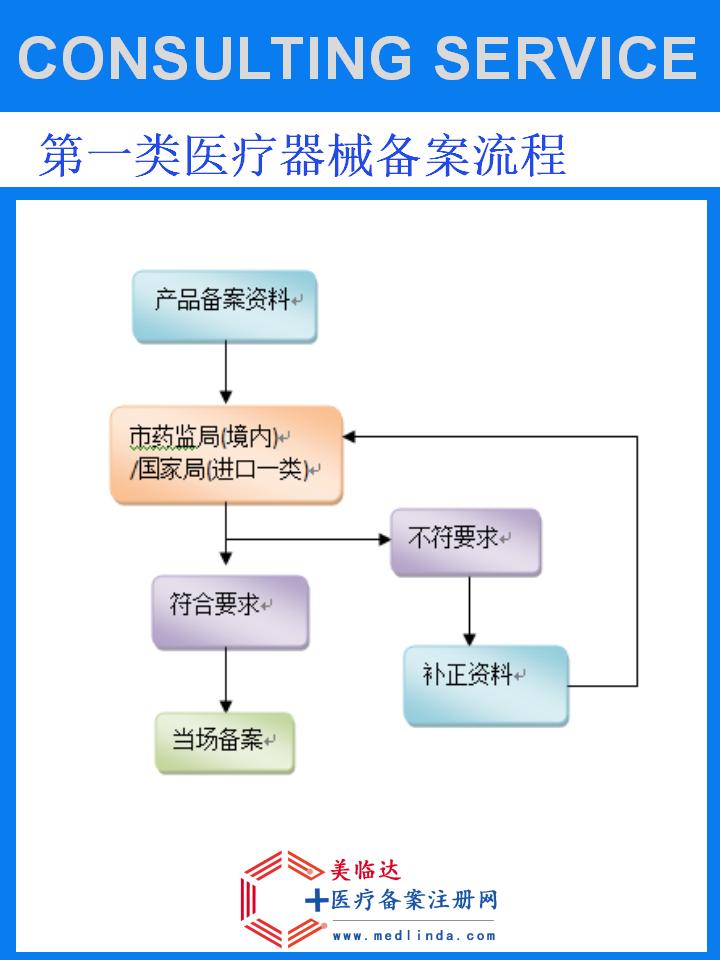
企业可根据自身情况和产品特性选择合适的申请途径。目前,进口医疗器械备案主要有两种途径:一是直接向NMPA提交申请,二是通过省级药品监管部门转报至NMPA。企业可根据自身资源和经验,选择最适合自己的申请方式。
完成资料准备后,企业需按照要求将申请资料提交至指定部门。随后,进入审核阶段。NMPA将对提交的资料进行全面审查,包括资料的真实性、完整性、合规性等方面。审核过程中,NMPA可能会要求企业提供补充资料或进行现场检查。企业应积极配合,确保审核顺利进行。
经过审核,如产品符合相关要求,NMPA将颁发进口医疗器械备案凭证。企业收到备案凭证后,即可在中国市场合法销售该产品。
某国际知名医疗器械制造商,在将其先进的口腔科手术器械引入中国市场时,采用了专业的申请策略。企业首先成立了专门的备案团队,负责政策研究、资料准备和沟通协调工作。在资料准备阶段,企业充分利用了内部资源和外部专业机构的帮助,确保了资料的完整性和准确性。同时,企业还积极与NMPA沟通,了解审核流程和注意事项,避免了不必要的延误和错误。最终,在团队的共同努力下,企业成功获得了进口口腔科手术器械医疗器械备案凭证,并顺利将产品推向了中国市场。
随着全球医疗技术的快速发展和医疗健康需求的不断增长,医疗健康国际化趋势日益明显。进口口腔科手术器械作为国际医疗技术交流的产物之一,其备案申请过程也是医疗健康国际化的重要体现。企业应紧跟国际化步伐,加强与国际同行的交流与合作,共同推动医疗技术的进步与发展。
在医疗器械行业,合规经营是企业生存和发展的基石。进口口腔科手术器械的备案申请过程不仅是对产品质量的检验也是对企业合规经营能力的考验。企业应树立合规意识强化内部管理建立健全的合规体系确保产品从研发、生产到销售的每一个环节都符合法律法规的要求。同时企业还应加强员工培训提高员工的合规意识和能力确保企业在激烈的市场竞争中立于不败之地。
进口口腔科手术器械医疗器械备案凭证的申请过程虽然复杂但意义重大。企业需全面了解政策与法规精心准备申请资料选择合适的申请途径并积极配合审核工作。同时企业还应关注医疗健康国际化和医疗器械合规经营等热门话题不断提升自身的竞争力和市场适应能力。在未来的发展中进口口腔科手术器械有望在口腔医学领域发挥更加重要的作用并为企业带来更加广阔的发展前景。