 联系我们
联系我们
 18210828691
18210828691







【图文】牙科口外研磨材料一类医疗器械备案详解:轻松合规,守护口腔健康
#牙科口外研磨材料备案# #一类医疗器械合规# #口腔健康守护#
在牙科领域,口外研磨材料作为一类重要的医疗器械,广泛应用于牙齿修复、调整和清洁等过程中。为了确保牙科口外研磨材料的质量和安全性,符合相关法规要求,进行一类医疗器械备案成为了不可或缺的一环。本文将为您详细解析牙科口外研磨材料一类医疗器械备案的流程和要求,助您轻松合规,守护口腔健康。
一、牙科口外研磨材料一类医疗器械备案的定义
牙科口外研磨材料一类医疗器械备案是指按照国家药品监督管理局(NMPA)的相关规定,对牙科口外研磨材料产品进行备案登记,以确认其符合一类医疗器械的标准和要求。通过备案,企业可以合法生产、销售和使用牙科口外研磨材料,保障产品的质量和安全性。
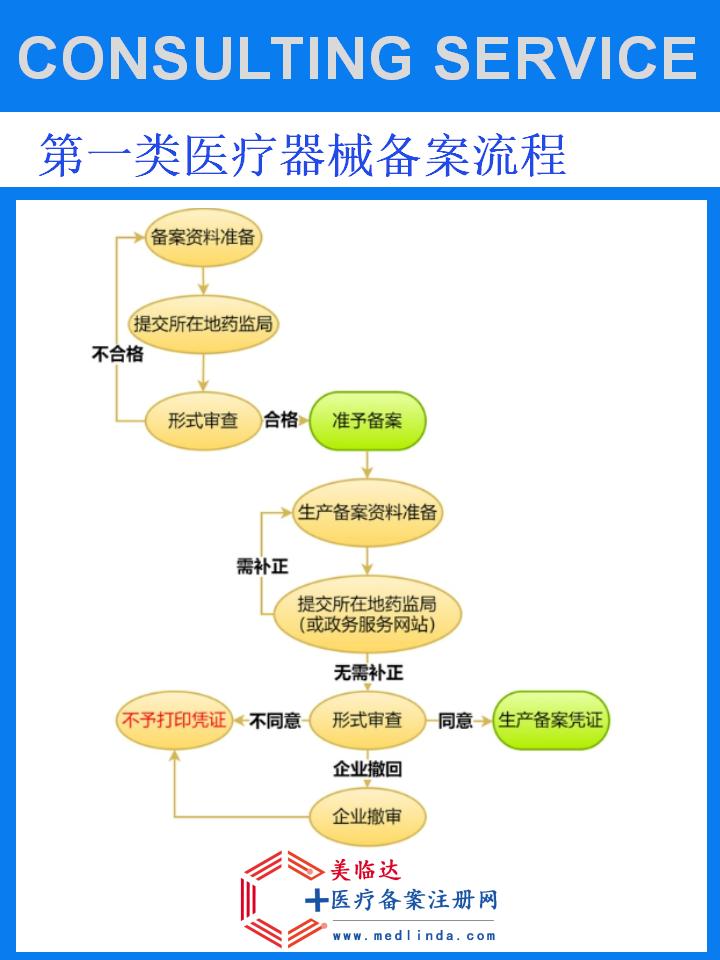
二、牙科口外研磨材料一类医疗器械备案的流程
在开始备案前,企业需要详细了解NMPA关于一类医疗器械备案的相关法规和政策要求,确保产品符合备案条件。
企业需要准备完整的备案资料,包括产品说明书、技术规格书、生产工艺流程图、原材料证明、检验报告等。这些资料将用于证明产品的安全性、有效性和合规性。
将准备好的备案资料提交至NMPA指定的备案机构或在线平台。在提交申请时,务必按照要求填写相关信息,如企业名称、产品名称、规格型号等。
备案机构将对提交的备案资料进行审核与评估。审核内容主要包括产品的技术性能、安全性、生产条件等方面。如有问题,备案机构将通知企业进行补正。
经过审核和评估后,如产品符合相关要求,备案机构将颁发牙科口外研磨材料一类医疗器械备案证书。企业凭此证书可合法生产、销售和使用牙科口外研磨材料。
三、牙科口外研磨材料一类医疗器械备案的注意事项
通过牙科口外研磨材料一类医疗器械备案,企业可以确保产品的质量和安全性,提升品牌形象和市场竞争力。同时,这也是对消费者口腔健康负责的表现。希望本文能为您的牙科口外研磨材料一类医疗器械备案提供有益的参考。