 联系我们
联系我们
 18210828691
18210828691







【图文】一次性使用止血带上市资质办理指南
在现代医疗领域,一次性使用止血带作为手术和急救过程中不可或缺的辅助器材,其质量和安全性对于保障患者生命安全至关重要。为了确保市场上销售的一次性使用止血带符合相关法规和标准,企业需要完成一系列的上市资质办理流程。本文将为您详细介绍一次性使用止血带上市资质的办理指南,帮助您顺利获得所需资质,为患者提供更安全、可靠的医疗产品。
#热门话题# 一次性使用止血带:守护生命,安全无忧
一、上市资质定义
上市资质是指医疗器械生产企业在产品上市前,必须按照国家相关法规和标准要求,通过一系列的程序和审核,获得允许在市场上销售产品的资格。对于一次性使用止血带而言,获得上市资质意味着该产品已经通过了严格的质量控制和安全性评价,可以安全、有效地应用于医疗领域。
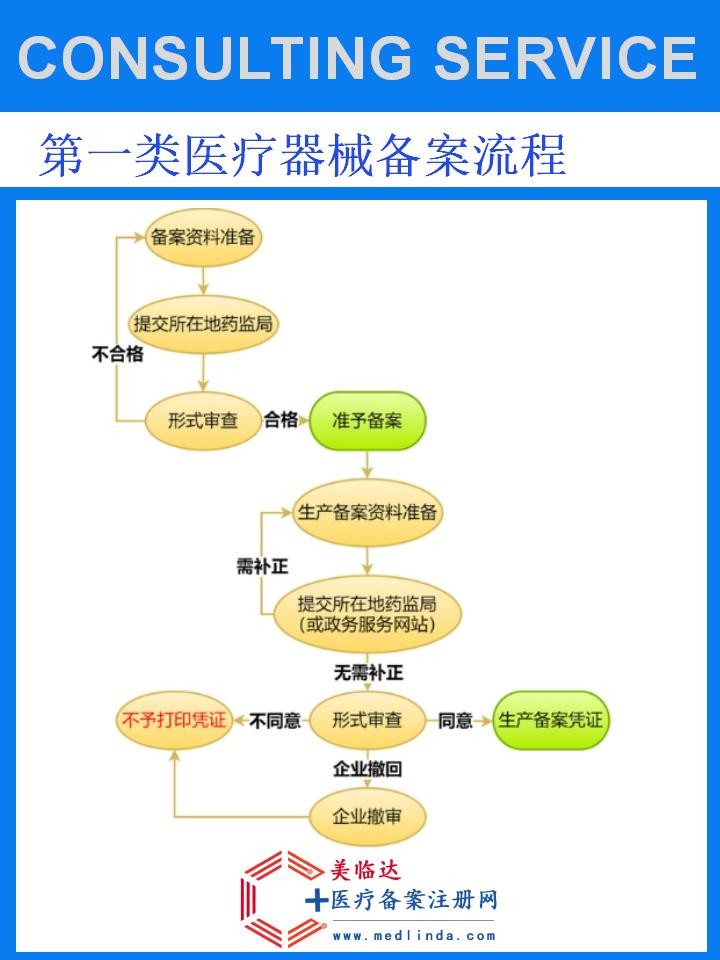
二、一次性使用止血带上市资质办理流程
在启动上市资质办理流程前,企业需要深入了解国家关于医疗器械的法规和标准,特别是针对一次性使用止血带的具体要求。这包括了解产品的分类、技术要求、临床试验等方面的规定,确保产品符合相关要求。
根据法规要求,企业需要准备以下申请材料:
企业将准备好的申请材料提交至当地医疗器械监管部门,并缴纳相应的申请费用。监管部门将对申请材料进行初步审核,确认材料齐全、符合要求后,受理企业的申请。
监管部门将组织专家对企业的申请材料进行技术审评,评估一次性使用止血带的性能、质量、安全性等方面是否符合要求。如有需要,监管部门还可能进行现场核查或要求企业补充材料。
经过技术审评和现场核查(如有),监管部门将向符合要求的企业颁发一次性使用止血带上市资质证书。企业凭此证书即可在市场上合法销售一次性使用止血带产品。
三、结语
一次性使用止血带上市资质的办理是确保产品合规性、保障患者安全的重要步骤。通过本文的介绍,相信您已经对上市资质办理流程有了更清晰的认识。让我们携手努力,为医疗行业的繁荣和健康贡献力量!