 联系我们
联系我们
 18210828691
18210828691


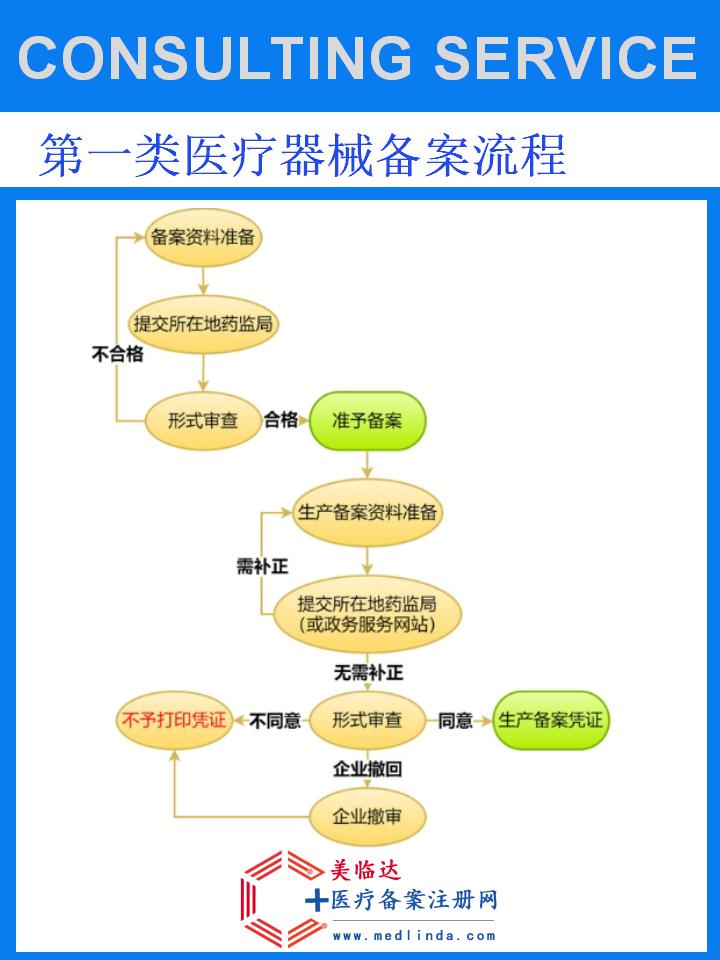





【图文】止血带生产备字号申请方法:解锁医疗器械市场的合规路径
在医疗领域,止血带作为手术中不可或缺的辅助工具,其质量和安全性直接关系到患者的生命安全与手术效果。随着#医疗质量与安全保障#成为行业内外关注的焦点,止血带生产企业需严格遵守国家相关规定,完成备字号(即医疗器械备案或注册证)的申请,以确保产品合法合规地进入市场。本文将为您详细解析止血带生产备字号申请的方法,助您轻松跨越合规门槛。
止血带,又称止血带或压力绷带,是一种用于控制出血、减少手术部位出血量的医疗器械。而备字号,则是国家对医疗器械实施分类管理,确保产品安全、有效、质量可控的重要手段。止血带作为医疗器械的一种,其生产企业需向国家药品监督管理局申请并获得相应的备案或注册证,即备字号。
首先,止血带生产企业需明确产品的具体分类(如一类、二类或三类医疗器械),因为不同类别的医疗器械在申请备字号时的要求、流程和材料有所不同。
根据产品分类和国家药监局的要求,准备齐全的申请材料。一般而言,申请材料包括但不限于企业资质证明、产品技术资料(如设计图纸、生产工艺、原材料证明、质量检测报告等)、产品使用说明书、临床评价资料(如适用)等。
将准备好的申请材料提交至所在地省级或国家药品监督管理局指定的受理窗口或在线平台。提交前,务必仔细核对材料的完整性和准确性,确保无遗漏或错误。
监管部门将对提交的申请材料进行形式审查,必要时进行现场核查或抽样检验。企业需积极配合监管部门的审核工作,及时提供补充材料或解答疑问。
经过审核,若产品符合相关法规和标准要求,监管部门将颁发备字号证书。企业收到证书后,即可合法生产、销售和使用该止血带产品。
通过遵循上述申请方法和注意事项,止血带生产企业不仅能够顺利获得备字号证书,还能在医疗器械市场中树立合规、专业的品牌形象,把握#医疗质量与安全保障#带来的发展机遇。